Znajdź zawartość
Wyświetlanie wyników dla tagów 'beta amylaza' .
-
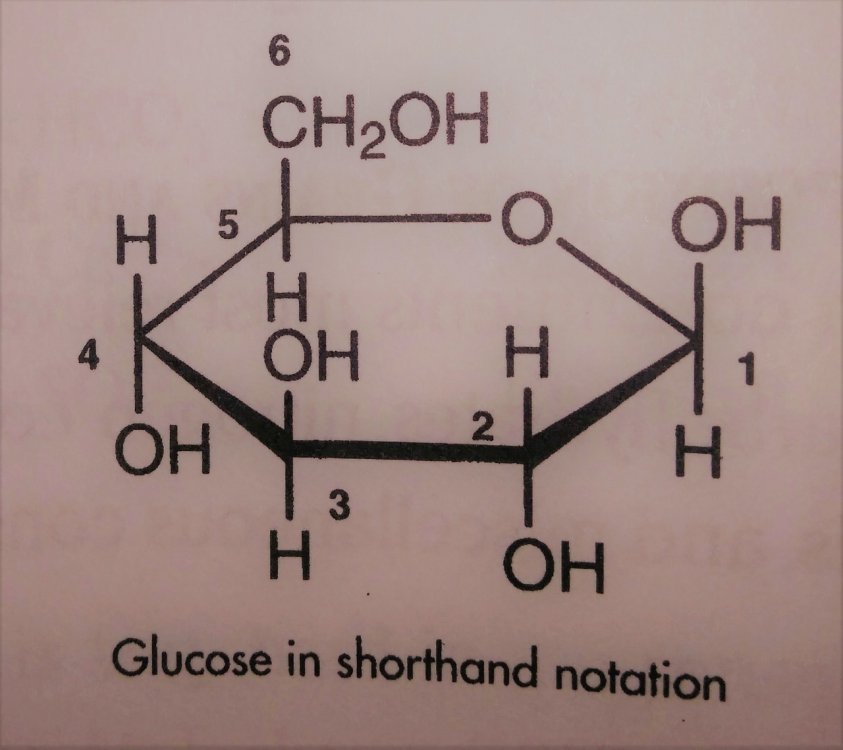
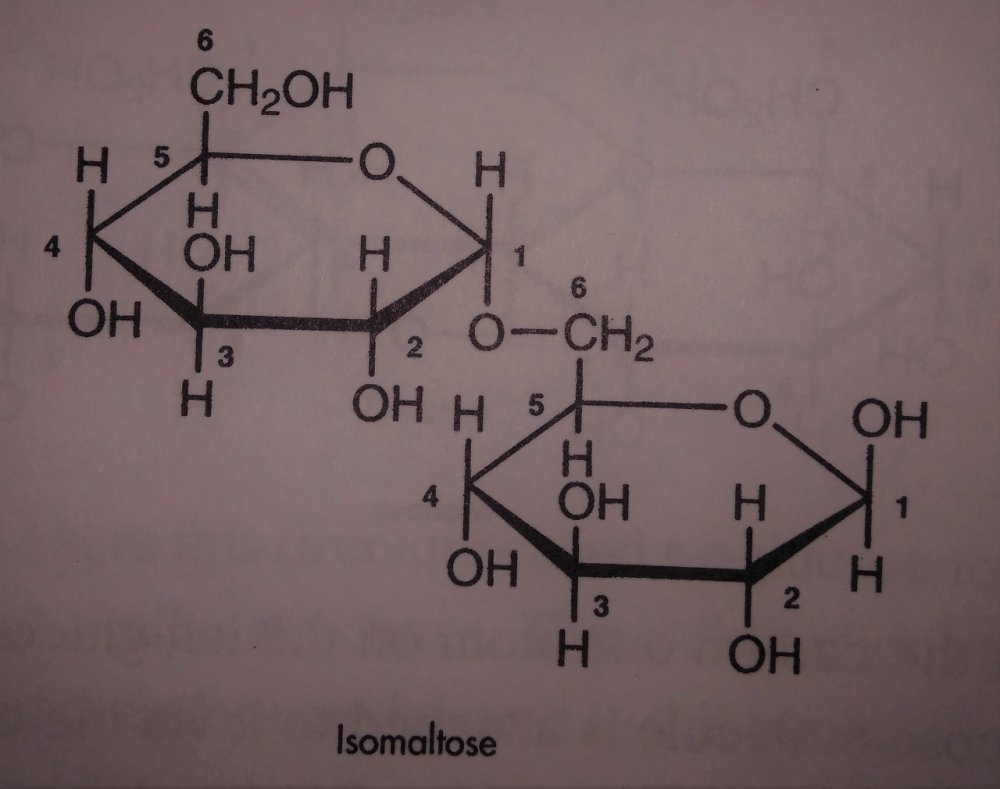
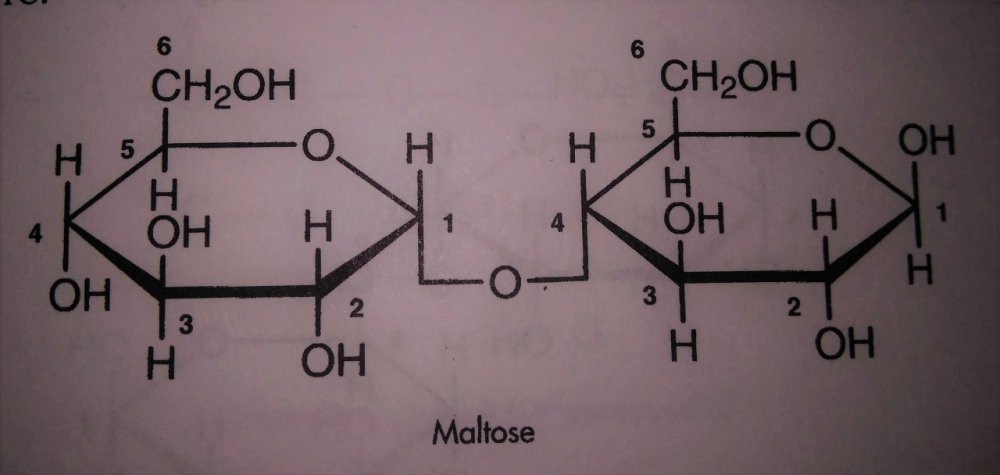
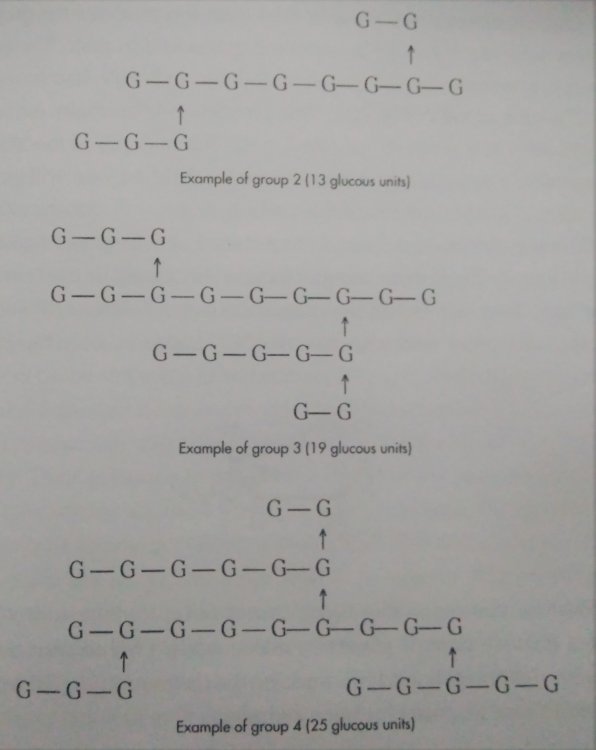
Skrobia i jej konwersja do cukrów prostych a przynajmniej prostszych. Zastanowiło mnie to pytanie kolegi @Fenris. I zrozumiałem, że nie rozumiem jak te enzymy tak naprawdę działają Nie dało mi to spać i sprawdziłem w tych źródłach. [1] Principles of Brewing Science : A Study of Serious Brewing [2] Skojarzylem, że moja ulubiona strona z temperaturami kleikowania jest w zasadzie o konwersji skrobi a kleikowanie to tylko jeden z etapów. [3] Nie mogło się obejść bez super artykułu o biochemii piwa Na sam koniec warto obejrzeć ten film, w którym jest to wyjaśnione w kilka minut. Wnioski spisuję poniżej, może komuś się przyda. W brzeczce mamy wiele cukrów, które w zasadzie prawie zawsze składają się z cząsteczek glukozy. Glukoza wygląda tak (zaczerpnięte z [1]): Te numerki oznaczają ponumerowane atomy węgla. Jako, że związki organiczne to związki węgla to literki C najczęściej się nie pisze. Na każdym z tych ‘skrzyżowań’ przy numerku jest atom węgla. Glukoza ma taką właściwość, że jest w stanie łączyć się w bardziej złożone cząsteczki. Jeżeli dołączymy do powyższej cząsteczki drugą. Połączymy ze sobą węgiel 1 z węglem 4 za pomocą tlenu to będziemy mieli maltozę. Dygresja pisząc wiązania mam na myśli wiązania alfa 'α'. Inne z punktu widzenia piwowara domowego są mniej ciekawe, bo tworza inne związki i wymagają innych enzymów do rozłożenia, których w brzeczce nie ma. Przykładem takiego innego cukru jest celuloza która zamiast wiązań alfa ma wiązania beta. Dodając kolejną cząsteczkę do szeregu (ponownie 1,4) będziemy mieli trójcukier nazwany maltotriozą. Dodając kolejne cząsteczki glukozy wiązaniem 1,4, i trochę upraszczając, zbuduje się długa nitka zwana amylozą. Zobaczcie, że dołączana jest cząsteczka glukozy zawsze po prawej stronie. Lewy koniec takiej nitki nazywa się nieredukujący prawy do którego dołączyliśmy cząsteczki to koniec redukujący. Będzie to ważna za chwilę. Amylozy, mogą się łączyć ze sobą i ich natura jest taka, że łączą się ze sobą za pomocą tlenu co 20-30 cząsteczek glukozy wiązaniem 1,6. To stanowi około 4% połączeń. Wiązanie takie wygląda tak (zaczerpnięte z [1]): Tylko te dwa rodzaje wiązań potrafią budować bardzo złożone struktury - amylopektyny. Przykładowo (zaczerpnięte z [1]): G - to cząsteczka glukozy. Myślniki między nimi to wiązania 1,4, strzałki w górę to wiązania 1,6. W rzeczywistości połączonych cząsteczek glukozy są ogromne ilości. Amylopektyny i Amyloza to w naszym rozumieniu skrobia. Po lewej stronie każdej z linii to koniec nieredukujący po prawej redukujący (tam może się doczepiać kolejna cząsteczka glukozy). Wkraczają nasi czterej bohaterowie, bardzo znani i lubiani: α-amylaza, β-amylaza, i mniej znani, teochę w cieniu, dekstrynaza graniczna oraz α-glukozydaza. Do tej pory myślałem, że α-amylaza jest w stanie rozerwać wiązanie 1,6. Oczywiście było to uproszczenie wyczytane w którejś z książek. Nie jest to jednak prawda. Wiązanie 1,6 jest w stanie rozciąć enzym dekstrynazy granicznej, stąd jej nazwa. Dekstrynaza graniczna jest niestabilna w temperaturach zacierania i wg artykułu [2] oraz [3]. W temperaturze powyżej 62.5°C staje sie coraz mniej znacząca. Właśnie dlatego mamy sporo dekstryn w piwie, ale to za chwilę. Zacierając w niskich temperaturach sporo tych wiązań zostanie rozbitych i w efekcie będzie bardziej fermentowalana brzeczka. Ale też mocno ją wytrawi za sprawą alkoholu. Dekstryny powodują, że piwo jest bardziej pełne w smaku. Dygresja, w How To Brew, Palmer określa piwa z dużą ilością dekstryn jako 'fart beers' Enzym α-glukozydaza (ang. maltase) ma optimum w zakresie 30°C - 40°C, powyżej 45°C ulega denaturacji (zniszczeniu) i nie jest już zdolny do pracy. A to co potrafi robić, to odcinać cząsteczki glukozy z końców nieredukujących. I kolejny problem. W takiej temperaturze nie zaszło jeszcze kleikowanie, skrobia nie została uwolniona. Ten enzym niewiele ma do roboty jak wrzuciłeś słód do wody o temperaturze 40°C. Chyba, że podzielimy zasyp, powiedzmy na pół. Część zatrzemy (bo najpierw się skleikuje) ponownie obniżymy temperaturę do 40 stopni i dodamy drugą część zasypu. Tak robią pszenicę w Weihenstephan (polecam spróbować na szczepie WY3068 Weihenstephan Weizen). Dodatkowa glukoza ma znaczny udział w produkcji estrów. Będzie zauważalnie więcej banana (dzięki @Undeath za materiały o tym) Wróćmy do znanych bohaterów. β-amylaza, potrafi rozbijać tylko wiązania 1,4 i odcinać dwie połączone cząsteczki glukozy czyli maltozę. Dodatkowo ma inne ograniczenia. Odcina tylko od strony końca nieredukującego oraz jak jest blisko wiązania 1,6 to nie potrafi się tam ‘wcisnąć’ i zostawia w efekcie kilka cząsteczek glukozy. Nie znalazłem ile dokładnie, na rysunkach w artykułach widać, że są to 2 cząsteczki glukozy przed wiązaniem 1,6, nie musi to być prawda. Zatem wydawałoby się, że szybko skończy i się zablokuje. Bo obedrze skrobię z wszystkich nieredukujących końców, dotrze do wiązań 1,6 i dalej stoi. Otóż nie, bo wchodzi α-amylaza, cała na biało. Taki berserker. Tnie wiązania 1,4 (i tylko te) na ślepo, losowo. To ona robi końce nieredukujące dla β-amylazy. Jest jeszcze jedna ważna sprawa. Enzym α-amylazy nie potrafi działać bez wapnia. Brzeczka mająca poniżej 50 mg/l wapnia nie zrobi dobrego piwa, Wapń jest również zawarty w słodzie, jasne słody mają go około 90mg/kg. Zalecane jest około 200 mg/l [1]. Z wapniem też nie ma co przesadzać, bo zrobi kolejne problemy, jak mętne piwo po nagazowaniu. Zauważyłeś, że jak podnosisz temperaturę to zacier staje się bardziej płynny po jakimś czasie. To właśnie α-amylaza rozcinając długie łańcuchy na krótsze i powoduje upłynnienie zacieru. Kolejne ograniczenie α-amylazy to to, że nie potrafi odcinać pojedynczych cząsteczek glukozy, oraz kończy działanie przynajmniej jedną cząsteczkę przed wiązaniem α-1,6 Tak wygląda tabla optymalnej pracy poszczególnych enzymów: Enzym Temperatura °C pH α-glukozydaza 30 - 40 ~6 dekstrynaza graniczna 60-62.5 5,5 β-amylaza 60-65 5.4-5.6 α-amylaza 72-75 5.6-5.8 We wszystkich przypadkach wypadkowe pH wynosi około 5.5. Wypadkową temperaturą dla β-amylazy i α-amylazy jest zakres od 65 - 68°C. Dlaczego tak?Ponieważ w temperaturze 69°C β-amylaza stanie się nieaktywna po kilku-kilkunastu minutach [2]. Pozwoliłem sobie pożyczyć obrazek z [2], aby to wszystko zwizualizować. Podsumowując. Niebieskie strzałki to β-amylaza, odcina maltozę od końca nieredukującego i nie jest w stanie podejść bliżej jak na dwie cząsteczki glukozy od wiązania 1,6. Enzym czerwony to α-amylaza tnie losowo. To odetnie maltozę, to maltotriozę, to jakiś dłuższy łańcuch. Po odcięciu jest duża szansa, że będzie nowy koniec nieredukujący dla β-amylazy, w efekcie szybciej się będzie zacierało. Dekstrynaza graniczna (zielona) w wyższych temperaturach ma małe szanse na działania i w efekcie zostawi większość wiązań 1,6. To będą bardziej złożone i niefermentowalne cukry, dekstryny. Również jak nie pozwolimy β-amylazie zbyt długo działać i podniesiemy temperaturę powyżej tych 70°C w efekcie szybko wyłączając ją. Następnie pozwolimy trochę podziałać α-amylazie, powiedzmy w 72°C, to otrzymamy więcej długich cukrów jak maltotrioza. Oraz jeszcze dłuższych, które są zbyt skomplikowane dla drożdży by je zjadły. Oczywiście jak będzie działała odpowiednio długo, to uszczupli trochę wapnia (bo potrzebuje go do działania) i jest szansa, że wyprodukuje sporo więcej cukrów fermentowalnych. Tutaj już wchodzi warsztat i wyczucie piwowara. Dlatego też piwa zacierana w 74°C mają negatywną próbę jodową, są zatarte z punktu widzenia piwowara, chociaż mają mniej fermentowalnych cukrów. Jeszcze ciekawostka z [1]. Piwa które mają przerwę w 70-74 stopniach mają najczęściej lepszą pianę. Dzieje się tak na skórek łączenia krótszych białek z niektórymi dekstrynami. Optimum przypada na 72 stopnie. Jest to częsta temperatura w schematach zacierania. Została w zasadzie znaleziona empirycznie jako wynik obserwacji. Dopiero niedawno nauka znalazła potwierdzenie obserwacji. Na sam koniec mash-out, lub jak kto woli wygrzew. Dlaczego w 78°C? Dlatego, że gorąca woda może wypłukać jeszcze trochę skrobi, która się schowała gdzieś głębiej, powiedzmy w grubszych cząsteczkach śruty. W tej temperaturze α-amylaza jest jeszcze trochę aktywna. Zatem jest duża szansa, że zdąży tę skrobię resztkową rozłożyć. Skrobia jest niekorzystna w piwie. Powoduje jego zmętnienie i stanowi pożywkę dla bakterii. W długiej perspektywie bakterie mogą zacząć żyć i psuć piwo. To tyle, mam nadzieję, że się podobało. Zachęcam do przeczytania przynajmniej artykułów, które wymieniłem na początku. Tam jest to wyjaśnione bardziej szczegółowo. Jeżeli zauważyłeś błąd daj mi znać. Mam nadzieję, że nie pokręciłem pojęć i definicji podczas tłumaczeń. Nie jestem zawodowo związany z chemią/biochemią i wiele z tych pojęć było dla mnie nowe.
- 6 odpowiedzi